Onkologia

Pilnie pracujemy nad przełomowymi osiągnięciami naukowymi, które nie tylko mogą pozwolić przedłużyć życie, ale także je chronić. Ponieważ osoby chore na raka zasługują na więcej — więcej sposobów leczenia, lepszą jakość życia i więcej czasu.
Jesteśmy zaangażowani w rozwój terapii przeciwnowotworowych w ramach jednego z największych programów badawczo – rozwojowych w branży.
Dowiedz się więcej o kluczowych obszarach naszej działalności.
Czerniak
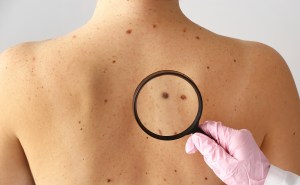
Czerniak jest poważną postacią raka skóry, a częstość występowania tej choroby w Polsce stale rośnie w ciągu ostatnich kilku dziesięcioleci.
Rozwija się w komórkach wytwarzających melaninę – pigment nadający kolor skórze, włosom i oczom. Uważa się go za najniebezpieczniejszą postać raka skóry ze względu na jego zdolność rozprzestrzenia się na inne części ciała, jeśli nie zostanie wcześnie wykryty i leczony.
Najczęstszym czynnikiem ryzyka rozwoju czerniaka jest narażenie na promieniowanie ultrafioletowe (UV) pochodzące ze słońca lub sztucznych urządzeń do opalania. Inne czynniki ryzyka obejmują jasną skórę, przebyte oparzenia słoneczne, rodzinną historię czerniaka, występowanie wielu znamion lub znamion nietypowych oraz osłabiony układ odpornościowy.
Wczesne wykrycie czerniaka ma kluczowe znaczenie dla powodzenia leczenia. Zaleca się regularne sprawdzanie skóry pod kątem pojawienia się nowych lub zmieniających się pieprzyków, a w przypadku zauważenia jakichkolwiek podejrzanych zmian należy niezwłocznie skonsultować się z lekarzem.
Czerniak może objawiać się w następujący sposób:
- płaskie brązowe plamy z postrzępioną krawędzią i małymi czarnymi plamkami,
- wypukłe brązowe plamy z różnymi kolorowymi plamami,
- twarde grudki w kolorze czerwonym, czarnym lub szarym.
Objawy czerniaka obejmują:
- zwiększenie rozmiaru znamienia,
- ciemnienie,
- stan zapalny,
- zmianę koloru,
- krwawienie oraz swędzenie,
- tkliwość lub ból w dotkniętym obszarze.
W wykryciu czerniaka pomaga tzw. reguła ABCDE. Opisuje ona cechy znamion, które mogą oznaczać czerniaka i jest pomocnym przewodnikiem w monitorowaniu zmian skórnych.
A – asymetria, np. znamię „wylewające” się na jedną stronę
B – brzegi poszarpane, nierównomierne, posiadające zgrubienia
C – czerwony, czarny, niejednolity kolor
D – duży rozmiar, wielkość zmiany powyżej 6 mm
E – ewolucja, czyli postępujące zmiany zachodzące w znamieniu czerniaka
Płuco

Na całym świecie rak płuca jest główną przyczyną zgonów z powodu nowotworów i odpowiada za ponad 18% wszystkich zgonów z tego powodu. Rak płuca jest w Polsce wykrywany u ponad 22 tys. osób rocznie. Zabija on prawie tyle samo osób, co trzy kolejne najczęstsze nowotwory łącznie: piersi, prostaty i jelita grubego.
Najczęstszą przyczyną raka płuca jest palenie tytoniu, w tym papierosów, cygar i fajki. Jednkaże 10-20% chorych na raka płuca nigdy nie paliło. Inne czynniki ryzyka obejmują narażenie na radon, azbest, niektóre chemikalia i obciążenia wynikające z historii raka płuca w rodzinie.
Objawy raka płuca mogą być różne, ale mogą obejmować one: uporczywy kaszel, ból w klatce piersiowej i barku, duszność, chrypkę, niezamierzoną utratę wagi i odkrztuszanie krwi. Wczesna diagnoza i leczenie mogą poprawić wyniki leczenia, dlatego ważne jest, aby zwrócić się o pomoc lekarską, jeśli pojawią się jakiekolwiek niepokojące objawy.
Niskodawkowa tomografia komputerowa (NTDK) – bezpieczne i krótkie badanie diagnostyczne, może być niezwykle pomocne w przypadku wykrycia zmian rakowych w płucu na wczesnym etapie, gdzie możliwa jest cała paleta działań terapeutycznych, z operacją włącznie.
Głowa i szyja

Nowotwory głowy i szyi rozwijają się zwykle w błonie śluzowej górnych dróg oddechowych – najczęściej w jamie ustnej, gardle i krtani, ale dotyczą ponad 30 lokalizacji w ciele. Wpływają na najważniejsze funkcje życiowe: połykanie, oddychanie oraz mowę.
W Polsce ok. 5,5 do 6 tys. pacjentów rocznie choruje na nowotwory w obrębie szyi i głowy.
Chodzi o grupę nowotworów wywodzących się z komórek płaskonabłonkowych wyścielających wilgotne powierzchnie wewnątrz głowy i szyi, w tym jamę ustną, gardło, jamę nosową i krtań. Nowotwory te występują częściej u osób po 50. roku życia i często są powiązane z czynnikami ryzyka, takimi jak palenie tytoniu i alkohol, a także zakażenie wirusem brodawczaka ludzkiego (HPV).
Objawy raka głowy i szyi mogą obejmować uporczywe owrzodzenia w jamie ustnej lub gardle, trudności w połykaniu, zmianę głosu, guzek lub obrzęk szyi oraz niewyjaśnioną utratę wagi. Wczesne wykrycie ma kluczowe znaczenie dla powodzenia leczenia, a regularne kontrole stomatologiczne i lekarskie mogą pomóc we wczesnej identyfikacji wszelkich niepokojących objawów.
Przełyk

Jest to nowotwór złośliwy, który rozwija się w przełyku. Diagnozuje się go zwykle u osób starszych i częściej występuje u mężczyzn niż u kobiet.
Do głównych czynników ryzyka raka przełyku zalicza się długotrwały refluks żołądkowy (cofanie się treści żołądkowej do przełyku), palenie tytoniu, duże spożycie alkoholu, otyłość i niektóre czynniki dietetyczne.
Objawy raka przełyku mogą obejmować trudności w połykaniu, ból lub dyskomfort w klatce piersiowej, niewyjaśnioną utratę wagi, uporczywy kaszel, chrypkę lub niestrawność. Wczesne wykrycie jest ważne dla powodzenia leczenia, a osoby, u których wystąpią jakiekolwiek niepokojące objawy, powinny skonsultować się z pracownikiem służby zdrowia w celu ich oceny.
Ryzyko zachorowania jest większe u osób, które:
- palą lub piją alkohol,
- są zarażone wirusem HPV,
- miały raka głowy lub szyi,
- miały radioterapię przełyku w celu leczenia innych pobliskich nowotworów,
- miały nieleczoną chorobę refluksową przez wiele lat.
Jelito grube

Rak jelita grubego jest rodzajem nowotworu rozwijającego się w okrężnicy lub odbytnicy.
Rak jelita grubego jest trzecim najczęstszym nowotworem zarówno u mężczyzn, jak i u kobiet oraz drugą najczęstszą przyczyną zgonów spowodowanych nowotworami na świecie. W 2020 r. na całym świecie zdiagnozowano ponad 1,9 miliona nowych przypadków tego raka.
Uważa się, że 75% nowotworów jelita grubego występuje bez związku z czynnikami genetycznymi, a pozostałe przypadki są związane z predyspozycjami genetycznymi, wywiadem rodzinnym, czynnikami związanymi ze stylem życia, takimi jak dieta i aktywność fizyczna, oraz innymi schorzeniami.
Kluczem do zmniejszenia zachorowalności i śmiertelności związanej z rakiem jelita grubego jest jego wczesne wykrycie za pomocą badań przesiewowych, takich jak kolonoskopia, ponieważ może to pomóc w identyfikacji polipów przednowotworowych lub nowotworów we wczesnym stadium, gdy leczenie jest najbardziej skuteczne.
Pierś

Rak piersi jest najczęstszym typem nowotworu na świecie. Choroba ta ma wiele podtypów, w tym podtypy agresywne, takie jak potrójnie ujemny rak piersi, który stanowi 10–15% wszystkich przypadków raka piersi.
Potrójnie ujemny rak piersi odnosi się do podtypu raka piersi, w którym komórkom nowotworowym brakuje receptorów estrogenowych (ER) lub progesteronowych (PR) i nie produkują wcale lub w zbyt dużej ilości białka o nazwie HER2.
Potrójnie ujemny rak piersi jest bardziej agresywny i wiąże się z większym ryzykiem nawrotu w porównaniu z rakiem z dodatnimi receptorami hormonalnymi lub HER2-dodatnimi, często dotyka młodsze kobiety oraz osoby, u których w rodzinie występowała ta choroba.
Mammografia i badanie USG są częścią profilaktyki wtórnej raka piersi, mającej na celu wczesne wykrycie zmian nowotworowych. Obecnie tylko mammografia jest objęta Programem Przesiewowych Badań Profilaktycznych, który jest bezpłatny i nie wymaga skierowania. Badania te mogą wykazać zmiany, które nie są jeszcze wyczuwalne palpacyjnie.
Nie do przecenienia w profilaktyce raka piersi jest również regularne wykonywanie badania palpacyjnego piersi, zarówno to wykonywane samodzielne, jak i w gabinecie lekarskim.

Nerka

Rak nerkowokomórkowy to najczęstszy rodzaj raka nerki, stanowiący około 90% przypadków.
Objawy (najczęściej krwiomocz) zwykle nie rozwijają się, dopóki guz nie będzie duży lub nie będzie przerzutów, dlatego często zdarza się jego przypadkowe wykrycie.
Do czynników ryzyka zalicza się:
- wiek,
- palenie tytoniu,
- otyłość,
- wysokie ciśnienie krwi,
- występowanie raka nerki w rodzinie,
- leczenie niewydolności nerek (długoterminowa dializa).
Najczęstszym objawem jest duży lub mikroskopijny krwiomocz, po którym następuje ból w okolicy lędźwiowej, gorączka niewiadomego pochodzenia i wyczuwalny guz. Inne niespecyficzne objawy mogą obejmować zmęczenie, utratę wagi i wczesne uczucie sytości.
Szyjka macicy

Rak szyjki macicy to rodzaj nowotworu, który występuje w komórkach szyjki macicy, czyli dolnej części macicy łączącej się z pochwą.
Rak szyjki macicy jest w skali świata czwartym pod względem częstości występowania nowotworem u kobiet. Rocznie zapada na niego około 570 tysięcy kobiet.
Rak szyjki macicy jest spowodowany głównie przetrwałą infekcją wirusem brodawczaka ludzkiego (HPV) wysokiego ryzyka, bardzo często przenoszonym drogą płciową.
Regularne badania przesiewowe za pomocą cytologii lub testów HPV, w połączeniu ze szczepieniem przeciwko HPV mogą znacznie zmniejszyć ryzyko zachorowania na raka szyjki macicy lub wykryć go we wczesnym stadium, gdy jest on w dużym stopniu uleczalny.
Rak szyjki macicy to jedna z form raka, której najłatwiej zapobiegać i którą można leczyć, a mimo to pozostaje poważnym problemem zdrowotnym na świecie.
Więcej o zakażeniu HPV dowiesz się na stronie www.hpv.pl
Cytomegalia (wirus CMV)/ HEMATOONKOLOGIA

Cytomegalowirus (CMV) to powszechny wirus herpes, który może zarażać wiele osób na całym świecie. Chociaż większość osób z prawidłowo działającym układem odpornościowym nie wykazuje objawów zakażenia CMV, wirus pozostaje w organizmie w postaci utajonej.
CMV może jednak powodować poważne powikłania u osób z osłabionym układem odpornościowym, takich jak osoby zakażone wirusem HIV/AIDS lub przechodzące przeszczepy narządów.
Zakażenie CMV może być przenoszone drogą kontaktu z płynami ustrojowymi, takimi jak ślina, mocz, nasienie, mleko matki oraz transfuzje krwi.
Często występuje również zakażenie wewnątrzmaciczne płodu, gdy kobieta jest zakażona CMV w czasie ciąży. To może prowadzić do poważnych powikłań u noworodków, takich jak zaburzenia słuchu lub inne wady rozwojowe.
Objawy zakażenia CMV u osób z osłabionym układem odpornościowym może powodować:
- gorączkę,
- zmęczenie,
- zapalenie płuc wywołane przez CMV (duszność, kaszel, bóle mięśni, osłabienie),
- zapalenie siatkówki wywołane przez CMV (niewyraźne widzenie lub utrata wzroku),
- zapalenie żołądka lub jelit wywołane przez CMV (ból żołądka, krew w stolcu, nudności, wymioty, biegunka),
- zapalenie mózgu wywołane przez CMV (drgawki, bóle głowy, dezorientacja).
Diagnoza zakażenia CMV opiera się zazwyczaj na badaniach laboratoryjnych, które wykrywają obecność specyficznych przeciwciał CMV lub DNA wirusa.
W ciężkich przypadkach zakażenia CMV, szczególnie u osób z osłabionym układem odpornościowym, stosuje się leki przeciwwirusowe. Ważne jest również przestrzeganie zasad higieny, takich jak regularne mycie rąk czy unikanie kontaktu z objawami infekcji.
Badania nad opracowaniem szczepionek przeciwko CMV są w toku, zwłaszcza w celu ochrony kobiet w ciąży i ich dzieci przed wrodzonym zakażeniem CMV.
Infekcja wirusem CMV jest szczególnie dużym problemem dla osób po allogenicznym przeszczepie szpiku. Z racji bardzo niskiej odporności u takich osób, zakażenie wirusem może wywołać cytomegalię, która zagraża ich życiu. Prowadzi ona do zgonu ok. 50 proc. pacjentów z tym problemem. Należy pamiętać, że dla tej grupy chorych dostępna jest profilaktyka przeciwko zakażeniom CMV. Dzięki niej zakażenie CMV przestałoby być główną przyczyną wpływającą na śmiertelność w tej grupie pacjentów.
Jeśli masz pytania dotyczące zakażenia cytomegalowirusem, skonsultuj się z lekarzem lub specjalistą chorób zakaźnych. Pamiętaj, że w przypadku osób z osłabionym układem odpornościowym, takich jak pacjenci z HIV/AIDS lub po przeszczepieniu narządu, regularne monitorowanie i leczenie są kluczowe dla zapobiegania powikłaniom związanym z CMV.
Immunoterapia

Czym jest immunoterapia?
Na przestrzeni lat poczyniono ogromne postępy w badaniach nad rakiem, w wyniku czego immunoterapia stała się ważną terapią w leczeniu raka, zarówno jako samodzielne leczenie, jak i w połączeniu z innymi terapiami nowotworowymi.
W przeciwieństwie do leczenia miejscowego jakim jest chirurgia i radioterapia, immunoterapia kwalifikowana jest jako leczenie systemowe, polegające na podaniu leków ogólnoustrojowych. Do leczenia systemowego zaliczamy też: chemioterapię, hormonoterapię oraz leczenie celowane.
Immunoterapia jest innowacyjną opcją leczenia. Dzięki immunoterapii do walki z nowotworem aktywowany jest własny układ odpornościowy organizmu.
Immunoterapia to terapia lekowa podawana w postaci wlewu, która dociera do całego organizmu. Terapia nie jest nakierowana bezpośrednio na guz, ale raczej na aktywację własnego układu odpornościowego organizmu do walki z komórkami nowotworowymi.
Niektóre komórki nowotworowe mogą ukrywać się pod zdrowymi komórkami lub spowalniać naturalną odpowiedź immunologiczną organizmu. Immunoterapia powoduje, że komórki układu odpornościowego organizmu rozpoznają pewne cząsteczki na powierzchni komórek nowotworowych i atakują „zakamuflowane” komórki nowotworowe.
Immunoterapię można łączyć z chemioterapią w celu zwalczania raka. Dzieje się tak dlatego, że te dwie różne metody leczenia mogą wzajemnie wzmacniać swoje działanie. Terapię skojarzoną podaje się w postaci wlewu pod nadzorem lekarza.
Aby pomóc Ci zrozumieć, czym jest i jak działa immunoterapia, obejrzyj poniższy film.
Jak immunoterapia może Ci pomóc walczyć z rakiem?
Istnieje kilka różnych sposobów, w jakie lekarze mogą wzmocnić odpowiedź twojego układu odpornościowego, aby pomóc organizmowi w walce z rakiem.
Lekarze mogą:
- Podawać laboratoryjnie wytworzone wersje przeciwciał, które mają za zadanie namierzać i niszczyć komórki rakowe.
- Pobrać komórki (białe krwinki) z twojego własnego układu odpornościowego, rozmnożyć je w laboratorium i ponownie wprowadzić do organizmu.
- Podawać substancje, które sprawiają, że twój układ odpornościowy staje się bardziej sprawny w wykrywaniu i zabijaniu konkretnych komórek rakowych.
- Podawać leki, które mogą osłabić obronną reakcję, jaką komórki nowotworowe mają przeciwko układowi odpornościowemu.
Kiedy lekarze korzystają z komórek z własnego układu odpornościowego pacjenta, czasami stosują komórki, które już potrafią atakować raka, a czasami modyfikują komórki, aby były bardziej skuteczne. Większość terapii immunologicznych działa tylko na kilka rodzajów nowotworów.
Kiedy stosuje się immunoterapię?
Immunoterapię możemy stosować na różnych etapach leczenia. Oczywistym celem każdej terapii onkologicznej jest wyłapanie zmian nowotworych na takim etapie, aby możliwe było przeprowadzenie zabiegu chirurgicznego, który pozostaje jednym z podstawowych sposobów leczenia raka.
W większości przypadków immunoterapia raka pełni rolę uzupełniającą do stosowanego standardowo leczenia chirurgicznego, chemioterapii czy radioterapii.
Stosuje się ją wówczas w celu:
- Zmniejszenia guza przed operacją, wówczas mówimy o terapii neoadjuwantowej (wstępnej).
- Zniszczenia pozostałych komórek nowotworowych, zmniejszając w ten sposób ryzyko nawrotu choroby – wtedy mówimy o terapii adjuwantowej.
- Podniesienia komfortu i jakości ich życia chorych. Immunoterapia podawana w stadium zaawansowanym nowotworu jako leczenie objawowe (paliatywne) stara się opóźnić progresję choroby oraz przedłużyć życie chorych.
Stosowanie immunoterpii
Immunoterapia może być stosowana jako:
- monoterapia, co oznacza,że wykorzystuje się tylko jeden lek immunoterapeutyczny, a nie kombinację różnych terapii,
- terapia skojarzona, np. z chemioterapią lub terapią celowaną lub podwójną immunoterapią.
Decyzja o rozpoczęciu immunoterapii jest podejmowana przez lekarza specjalistę onkologii klinicznej, który na podstawie oceny klinicznej pacjenta oraz spełnieniu kryteriów programu, podejmuje decyzję o rozpoczęciu leczenia immunologicznego. Lekarz monitoruje również postęp leczenia i reakcję pacjenta na terapię, aby ustalić dalsze działania
W ramach programów lekowych, immunoterapia jest dostępna dla pacjentów z różnymi rodzajami nowotworów, takimi jak m.in. rak płuca, czerniak, rak szyjki macicy czy rak piersi. Kryteria kwalifikacji są ustalone w oparciu o wyniki badań histopatologicznych, które potwierdzają obecność konkretnego rodzaju nowotworu, oraz na podstawie oceny zaawansowania choroby, która może być dokonana na podstawie badań obrazowych, takich jak tomografia komputerowa czy rezonans magnetyczny. Dodatkowo, wyniki badań laboratoryjnych, takie jak obecność czynników predykcyjnych, poziom markera nowotworowego, czy funkcji narządowych, również są brane pod uwagę przy kwalifikacji do immunoterapii.

ZALETY STOSOWANIA IMMUNOTERAPII
Do niewątpliwych zalet immunoterapii nowotworów należy stosunkowo mała inwazyjność leczenia oraz akceptowalna toksyczność. Leczenie immunologiczne pobudza i wzmacnia odpowiedź układu odpornościowego, który precyzyjnie nakierowuje czynniki terapeutyczne w miejsca zmienione chorobowo.
Leki immunokompetentne nie uszkadzają zdrowych tkanek i narządów, jak ma to miejsce w przypadku tradycyjnej chemioterapii.
Zalety:
- Immunoterapia wykazuje zdolność do zapewnienia trwałych efektów, co oznacza, że działanie może być długotrwałe – utrzymują się nawet po zakończeniu leczenia.
- Niszczy wiele typów nowotworów i w wielu przypadkach może zapobiegać ich nawrotom.
- Może zapobiegać rozprzestrzenianiu się wielu rodzajów raka.
- Wzmacnia układ odpornościowy, dzięki czemu nadal walczy z rakiem nawet po zakończeniu leczenia.
- Powoduje działania niepożądane, które są zazwyczaj mniej poważne niż te związane z bardziej tradycyjnymi metodami leczenia raka, takimi jak chemioterapia.
- Wykazuje się potencjałem kombinacji, co oznacza, że można ją łączyć z innymi metodami leczenia nowotworowego, takimi jak chemioterapia, radioterapia czy terapie ukierunkowane.
Należy pamiętać, że chociaż korzyści te zaobserwowano w badaniach klinicznych, indywidualna odpowiedź na immunoterapię może się różnić.
Działanie niepożądane
Jak każdy lek, immunoterapia może powodować działania niepożądane. Mogą one czasami być poważne i wystąpić w dowolnym momencie leczenia lub nawet po jego zakończeniu.
Immunoterapia różni się od innych leków stosowanych w leczeniu raka, takich jak chemioterapia, ponieważ może powodować atak układu odpornościowego na zdrowe komórki. Może to prowadzić do tak zwanych „działań niepożądanych o podłożu immunologicznym”, które mogą wystąpić w dowolnym momencie leczenia, a czasem nawet po jego zakończeniu.
Pacjenci powinni być świadomi, jakie mogą wystąpić działania niepożądane stosowania immunoterapii i jak można sobie z nimi poradzić. Ważne jest, aby mieć pełną wiedzę na temat potencjalnych działań niepożądych i aby móc monitorować swoje samopoczucie oraz powiadomić lekarza, jeśli wystąpią jakiekolwiek niepożądane reakcje.
Aby dowiedzieć się więcej o możliwych działaniach niepożądanych, obejrzyj poniższy film.
Niniejszy materiał został dostarczony przez MSD Polska Sp. z o.o. jako ogólna informacja dla pacjentów. Pierwszym źródłem informacji na temat Pana/Pani stanu zdrowia i przebiegu leczenia powinien być lekarz prowadzący, dlatego w razie jakichkolwiek pytań dotyczących stanu zdrowia i przebiegu leczenia proszę zwrócić się do swojego lekarza.
PL-NON-01383 07/2024
